Презентация на тему: "Kémiai egyensúly 1. Spontán kémiai reakciók a Δ r G reakció-szabadentalpia előjele kijelöli a reakció irányát, a Δ r G=0 reakció-szabadentalpia minimum.". Скачать бесплатно и без регистрации.

Általános kémia tétel - 6. tétel Híg oldatok törvényei. Kolligatív sajátságok. Elektrolitok - Studocu
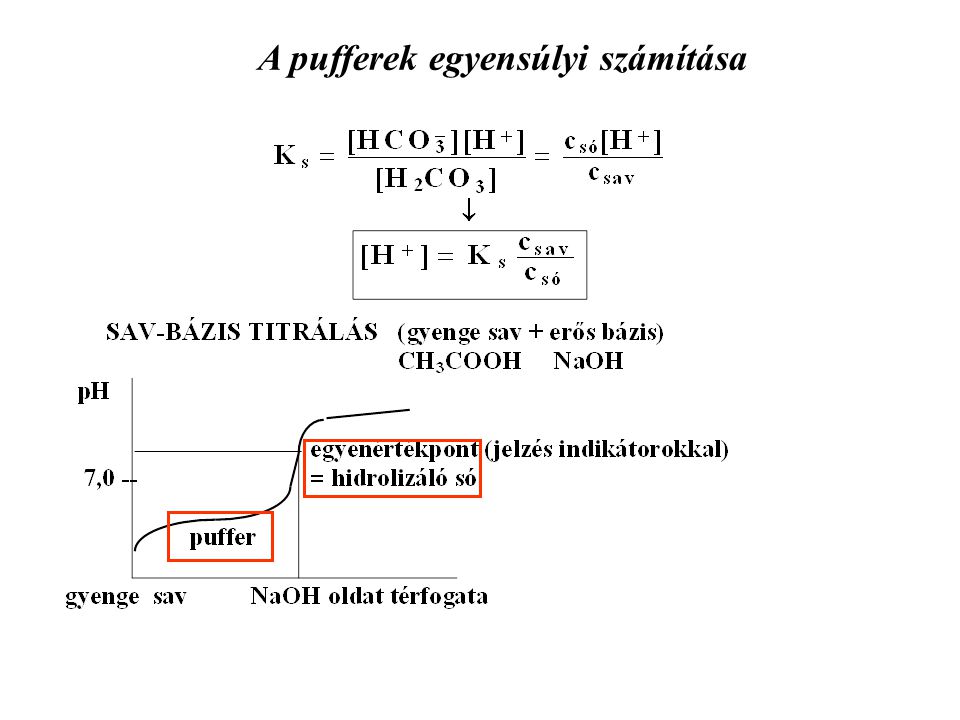
A KÉMIAI EGYENSÚLY A REAKCIÓK MEGFORDÍTHATÓK. Tehát nem játszódnak le végig, egyensúly alakul ki a REAKTÁNSOK és a TERMÉKEK között. Egyensúlyban a termékekhez. - ppt letölteni
A kémia tudományának tárgya, módszerei. Mennyiségek, mértékegységek, mérés. Az atomelmélet fejlődése. Radioaktivit